 |
|
 |
Hauptseite |
 |
Übersicht |
 |
Chemie |
 |
Tipps |
 |
Erfahrungen |
 |
Meer |
 |
Software |
 |
Bauanleitungen |
 |
Links |
 |
|
 |
Awards |
 |
Datenschutz/Impressum |
 |
Kontakt |
 |
Echo |
 |
|
 Chemie - Aquariumchemie alles über Wasserwerte und deren Messung Fertigen und genaue, weiterentwickelte Test sowie günstigste Fotometer gibt es auf der Wasserpantscher-Shopseite
KH und pH Zusammenhänge zwischen Karbonathärte und pH-Wert Ich habe schon auf anderen Seiten erwähnt, dass man durchaus nicht mit hoher Karbonathärte und hoher (geregelter) CO2-Zufuhr zur Steuerung des pH-Wertes sein Becken fahren muss sondern auch (bei Beachtung der dort gegebenen Hinweise) mit geringer Karbonathärte einen neutralen pH-Wert erreichen kann und dann auch nur ganz geringe Mengen CO2 zur Pflanzendüngung anwenden braucht. Karbonate sind in der Karbonathärte zwar enthalten, würden sie aber alleine für den sich daraus ergebenden pH-Wert zuständig sein, so wäre der pH-Wert viel zu hoch: 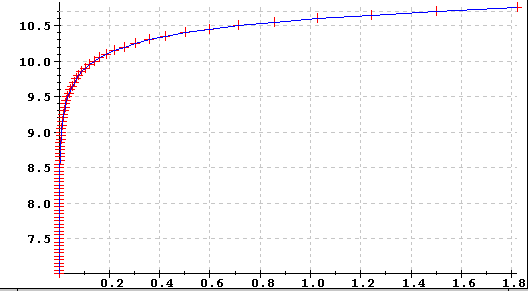 Beim Wet 1.0 der X-Achse wäre eine 0,001 Molare Karbonatkonzentration bei einem pH-Wert von über 10.5 ! Tatsächlich enthält unser Aquariumwasser (auch Leitungswasser) hauptsächlich Bikabonate (Hydrogenkarbonate) welche einen geringeren pH-Wert ergeben: 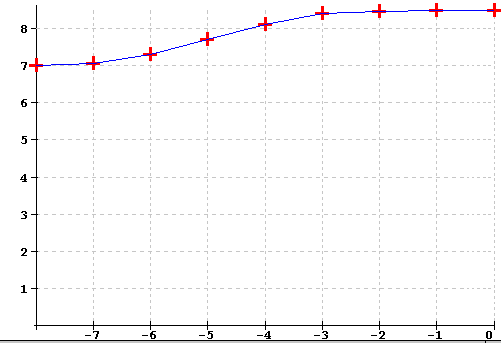 Wobei auf der X-Achse der Wert 0 (10 hoch Null) einer ein-molaren und der Wert -7 (10 hoch minus 7) einer 0,0000001-molaren Konzentration entspricht. Bei einigen KH-Graden haben wir etwa eine 0,001molare Konzentration (Wert -3) was bei Natriumhydrogenkarbonat (Natron) etwa 84 mg pro Liter entspricht und so einen pH-Wert von etwas über 8 ergibt. Man sieht auch, dass bei Karbonathärte Null, der pH-Wert auf minimal 7 (neutral) sinken kann (ohne andere Säuren im Wasser). Die nächste Grafik zeigt, wieviel 0.1 - molare Salzsäure (oder entsprechend konzentrierte andere Säure oder auch entsprechende Kohlensäure) man aufwenden muss um einen anderen pH-Wert zu erreichen wobei ein 100-Liter-Becken und eben die o.a. etwa 84 mg/l Natriumhydrogenkarbonat angenommen werden wobei die X-Achse (Waagrechte) diesmal den pH-Wert darstellt und durch die Messpunkte etwas verzerrt ist: 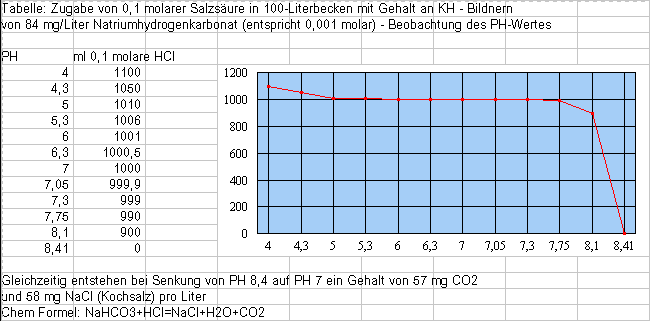 Was sofort auffällt ist die sogenannte "Pufferwirkung" der Karbonathärte. Um vom pH-Wert 8,41 auf 7,75 zu kommen braucht man 990 ml (also fast einen Liter) Säure, was bei den geregelten CO2-Anlagen zu hoher Verschwendung von CO2-führt um den pH-Wert zu drücken und für die Fische alles Andere als gut ist. Vom pH-Wert z.B.: 7,75 auf 7 braucht man nur 10 ml Säure, von 7,75 auf pH-Wert 5 (normalerweise die Untergrenze im Aquarium) braucht man nur 20 ml Säure, was zwar viel weniger ist als die vorher genannten 990ml aber die 20 ml Säure entstehen im Aquarium normalerweise nie. Auf den doch schon gefährlichen Wert von pH=4 sind dann schon bald 100 ml Säure notwendig, die erreicht man unmöglich im Aquarium. Man ersieht also, dass geringe Karbonathärte normalerweise nie zum so oft befürchteten "Säuresturz" führen wird, solange man nicht künstlich größere Mengen Säuren zuführt (vorher die Tabellen etc. mit Salzsäure waren nur ein Beispiel zur Erklärung der Größenordnungen). Für die CO2-Düngung braucht man nur geringste Mengen (Flaschenmethode reicht voll) und es ist, wie schon beschrieben, eine ausreichende Wasserbewegung/-Durchlüftung gegen die eventuelle Anhäufung von CO2 erforderlich. Auf periodischen Wasserwechsel wird man sowieso nicht verzichten. Man bewegt sich mit wenig Karbonathärte im pH-Bereich von 6.5 bis 7.5, bei geringer CO2-Düngung von 6 bis 7, was für die meisten Fische und Pflanzen ein Optimum darstellt. |
 Chemie Chemie |
 KH und pH KH und pH |
